I. Introdução: o que é, e quão comum é no Brasil
A lesão medular traumática acontece quando a medula espinhal sofre um dano por trauma — por exemplo, fratura e deslocamento de vértebras, compressão por fragmentos ósseos, hematoma, impacto direto ou ferimento por arma branca ou de fogo. Dependendo do nível (cervical, torácico, lombar) e da gravidade, ela pode causar fraqueza ou paralisia, perda de sensibilidade, alterações urinárias e intestinais, disfunção sexual e complicações autonômicas (pressão, sudorese, temperatura).¹
No Brasil, estimativas usadas em diretrizes nacionais apontam incidência aproximada de ~40 casos novos por milhão de habitantes/ano, o que corresponde a cerca de 6–8 mil novos casos por ano.¹
Principais causas no Brasil: as principais causas são acidente de trânsito (principalmente motociclistas, e pedestres), ferimento por arma de fogo, quedas (incluindo quedas de laje), e mergulho.¹
II. Tratamento inicial (fase aguda): por que rapidez e equipe especializada mudam o jogo
Os primeiros dias são decisivos por dois motivos:
- Evitar piora secundária: depois do trauma inicial, podem ocorrer inchaço, inflamação, falta de perfusão (pouco sangue) e compressão progressiva — fatores que agravam a lesão.²
- Tratar instabilidade da coluna: fraturas e luxações podem deixar a coluna instável; movimentações inadequadas podem piorar o dano neurológico.¹
Por isso, o ideal é que a pessoa seja avaliada o quanto antes em um serviço com experiência em trauma raquimedular, capaz de decidir (quando indicado) por:
- Descompressão (tirar a pressão sobre a medula/raízes)
- Estabilização (fixação para alinhar e “travar” a coluna)
- Cuidados intensivos, prevenção de trombose, manejo respiratório (sobretudo em lesões cervicais), controle de dor e monitorização neurológica.¹²
“Qual a chance de melhorar nos primeiros 3 meses?”
Isso depende muito do tipo de lesão (completa vs incompleta), nível, idade, rapidez do atendimento, e reabilitação. Mas há um dado importante para orientar expectativas: mesmo em lesões inicialmente completas (AIS A), uma parcela pode melhorar para algum grau de lesão incompleta com o tempo. Revisões de história natural mostram que cerca de 20–30% das pessoas inicialmente AIS A podem converter para incompleta (AIS B/C/D) ao longo do acompanhamento — e grande parte da recuperação neurológica e funcional tende a se concentrar nos primeiros meses, com redução progressiva do ritmo depois.³ Além disso, análises sobre conversão de gravidade sugerem que uma fatia relevante das mudanças ocorre precocemente (primeiras semanas/meses), embora a evolução varie bastante entre indivíduos.⁴
III. Tratamento das sequelas: reabilitação é tratamento (não “apenas fisioterapia”)
Depois da fase aguda, o foco muda: recuperar o máximo de função possível e evitar complicações. Em geral, os melhores resultados vêm de uma equipe com fisioterapia + terapia ocupacional + enfermagem especializada + urologia + controle de dor/espasticidade + psicologia, além do seguimento com neurocirurgia/ortopedia e fisiatria.¹
Abaixo, estratégias práticas por categoria:
a) Fisioterapia (movimento, força, marcha, condicionamento)
- Treino de transferências (cama–cadeira, cadeira–carro), equilíbrio sentado e em pé (quando possível).
- Fortalecimento de musculatura preservada + condicionamento cardiovascular (ergômetros, treino em cadeira, estimulação da musculatura com corrente elétrica ou campo magnético).
- Treino de marcha quando há indicação: barras paralelas, esteira com suporte parcial de peso, robótica/exoesqueleto (quando disponível).¹
b) Terapia ocupacional (autonomia no dia a dia)
- Adaptação de casa/banheiro, treino de atividades de vida diária (vestir-se, banho, cozinha).
- Tecnologias assistivas: utensílios adaptados, cadeira adequada, adaptações para dirigir/trabalhar.¹
c) Dor (nociceptiva e neuropática)
- Dor musculoesquelética: ajuste postural, adequação da cadeira, fortalecimento, manejo de sobrecarga de ombro.
- Dor neuropática (queimação, choque): costuma exigir abordagem combinada (medicamentos específicos, neuromodulação) e seguimento regular.¹²
d) Espasticidade (rigidez e “travamentos”)
- Alongamentos programados, posicionamento, ortóteses, fisioterapia diária.
- Em casos selecionados: medicamentos antiespásticos e, quando indicado, estratégias intervencionistas (Botox ou procedimentos neurocirúrgicos como bloqueios, neurotomias e por vezes até implante de bomba de medicamentos como Baclofeno).¹
e) Bexiga neurogênica
- Programas de esvaziamento programado (por exemplo, cateterismo intermitente), metas de segurança renal, prevenção de infecções e cálculo.¹
f) Intestino neurogênico
- Rotina intestinal (horários), ajuste de fibras e líquidos, técnicas de evacuação assistida, prevenção de impactação.¹
g) Prevenção de escaras (úlceras por pressão)
- “Alívios” de pressão (mudanças frequentes de posição), almofadas adequadas, inspeção diária da pele, nutrição e higiene.
- Atenção especial a calcâneos, sacro, ísquios e trocânteres.¹
IV. “Terapêutica armada”: órteses e robótica para ganho de função
Aqui entram recursos que “emprestam” estabilidade e movimento ao corpo — alguns mais simples, outros altamente tecnológicos:
Órteses mecânicas (puramente estruturais)
- Tornozeleiras (AFO), joelho–tornozelo–pé (KAFO), estabilizadores de tronco, adaptações para mão/punho, conforme o déficit.
Órteses eletro-mecânicas / com microprocessador
- Exemplos incluem soluções com controle de articulação para melhorar segurança e padrão de marcha. A Ottobock, por exemplo, tem órteses com articulação do joelho controlada (como a E-MAG Active), voltadas a pessoas que não conseguem estabilizar o joelho por fraqueza/paralisia de extensores.⁵
Exoesqueletos (robôs “vestíveis”)
- HAL (Cyberdyne): exoesqueleto que pode usar sinais do corpo/intenção de movimento para auxiliar marcha em reabilitação.⁶⁷
- Outros dispositivos usados em centros de reabilitação e/ou em cenários pessoais incluem plataformas como EksoNR (reabilitação) e linhas para SCI, e sistemas de uso pessoal (em perfis selecionados) como ReWalk, entre outros, com regulações e indicações específicas por país.⁸⁹
Importante: exoesqueleto não é “cura”, mas pode ser uma ponte para ganhos de condicionamento, controle postural, função em pé/marcha assistida, e até benefícios secundários (osso, circulação, intestino), dependendo do caso e do protocolo. Uma desvantagem desses sistemas, além do custo e baixa disponibilidade no país, é seu peso e dificuldade de ser usado em ambiente domiciliar (para além de centros de tratamento).
V. Estimulação medular (EES): a parte mais promissora
A estimulação elétrica epidural (EES) é uma forma de neuromodulação em que eletrodos são implantados no espaço epidural (próximo à medula) e conectados a um gerador. A ideia não é “substituir” a medula, mas recrutar e organizar circuitos remanescentes, facilitando a ativação muscular voluntária quando combinada com treino. Importante frisar que esse tratamento faz parte do rol de procedimentos da ANS (Agência Nacional de Saúde), e tem cobertura de custo em território nacional, atendidas algumas condições específicas.
a) Evidência em animais: efeitos de regeneração e plasticidade
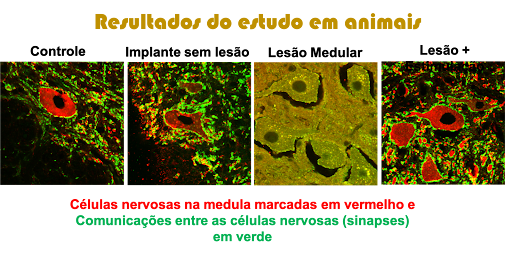
No nosso trabalho em modelo experimental (roedores), observamos que a estimulação epidural pode induzir efeitos de neuroproteção e plasticidade, com achados compatíveis com melhora do microambiente medular. Encontramos sinais de reorganização do tecido nervoso após a lesão, com indicadores de maior conectividade entre neurônios (sinapses) e maior número de células nervosas sobreviventes na medula lesada.¹⁰
Figura do nosso trabalho em ratos mostrando os efeitos benéficos da estimulação elétrica ao aumentar a quantidade de células nervosas viáveis e conexões sinápticas entre elas
b) Evidência em humanos: nosso estudo fase II
No estudo clínico fase II (análise interina) com 5 pacientes paraplégicos (ASIA A ou B) implantados e acompanhados por 12 meses, os resultados apontaram melhora objetiva em desfechos motores e funcionais.⁴⁽¹¹⁾
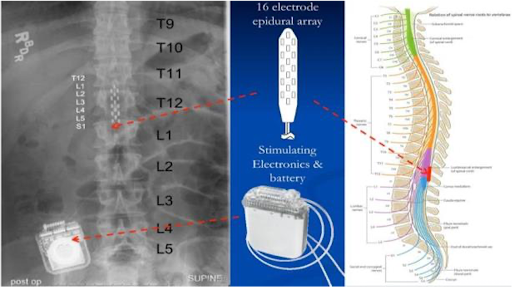
Figura ilustrando eletrodo implantado na coluna vertebral abaixo do nível da lesão (área laranja), e conexão ao respectivo gerador.
Principais pontos positivos reportados:
- Ganho motor significativo no escore Fugl-Meyer para membros inferiores (FMA-LE): média passou de 36 pontos para 55 pontos em 3 meses, 59 em 6 meses e 64 em 12 meses (uma melhora de 78%, que foi estatisticamente significativa).¹¹
- Eletromiografia (EMG) corroborou aumento de ativação voluntária.¹¹
- Houve melhora em equilíbrio e espasticidade.¹¹
- Segurança: não ocorreram eventos adversos graves ou moderados¹¹
Em linguagem simples, nesse grupo de pacientes crônicos com lesão grave (sem qualquer atividade muscular e após o período de melhora espontânea inicial do trauma), o estudo mostrou melhora mensurável e significativa da função motora, da ordem de 78%, com alto grau de segurança (sem piora relacionada ao tratamento).¹¹
c) Ensaios clínicos externos também sustentam eficácia
Esse resultado se alinha a outros estudos relevantes que demonstram eficácia da estimulação medular na lesão traumática, incluindo:
- Ensaio com treinamento baseado em atividade + EES mostrando melhora de desempenho de ficar em pé em lesão cervical.¹²
- Trabalho de referência em Nature Medicine mostrando restauração rápida de funções de tronco e perna em paralisia completa com neuromodulação dependente de atividade.¹³
VI. Futuros avanços: para onde isso está indo
a) Exoesqueletos mais inteligentes (com controle neural e melhor desenho biomecânico)
A tendência é integrar robótica com sinais biológicos (EMG/BCI), algoritmos adaptativos e materiais mais leves. Revisões e estudos na área de robótica em reabilitação indicam que o “como” (dose, intensidade, parâmetros do robô, seleção do paciente) influencia muito o resultado — e isso vale tanto para AVC quanto para lesão medular, porque o princípio é o mesmo: treino repetido, específico e bem dosado.¹⁴
Além disso, soluções como exoesqueletos de mão/órteses “soft” com acionamento por tendões e controle mais natural ilustram a direção do campo: conforto, compatibilidade articular e custo/benefício melhores.¹⁵
b) Transplante celular e terapias regenerativas (combinadas com neuromodulação)
A literatura evoluiu de “células como milagre” para uma visão mais realista: segurança, tipo celular, via de entrega, janela temporal e combinação com reabilitação/neuromodulação são determinantes. Uma revisão sistemática clássica do nosso grupo discutiu justamente esse panorama, indicando promessas e limites, e por que muitas estratégias ainda precisam de melhor evidência clínica.¹⁶
Outros trabalhos do grupo revisaram o estado da arte em humanos e também exploraram aplicações específicas como modulação de dor neuropática por meio de traansplantes celulares.¹⁷¹⁸
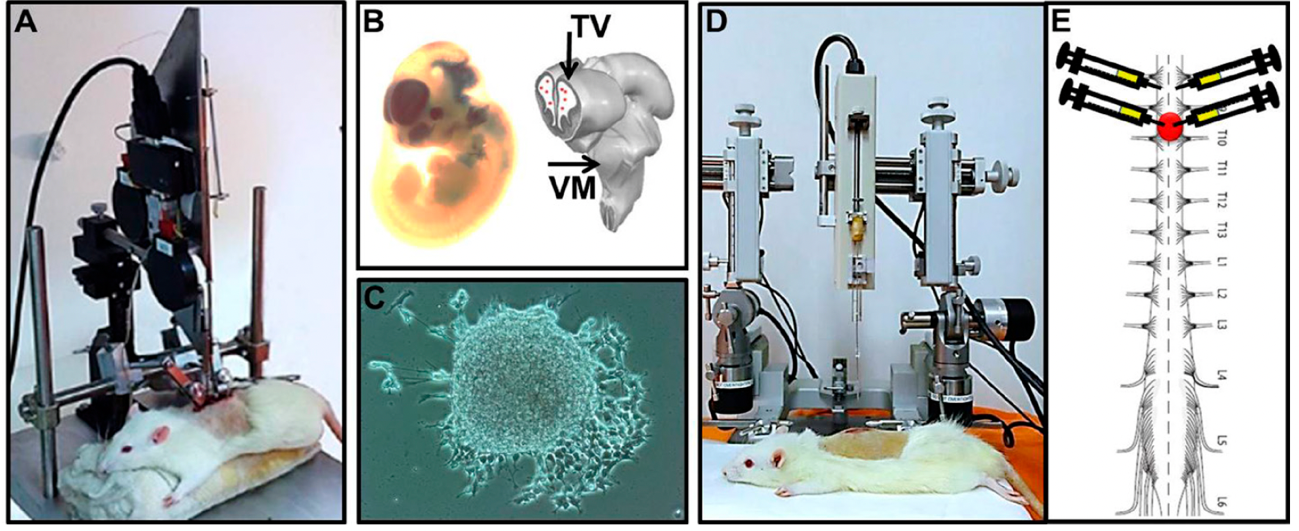
Figura ilustrando nosso estudo em ratos onde implantamos células-tronco neurais dentro da medula lesada por impacto
Referências
- Ministério da Saúde (BR). Diretrizes de Atenção à Pessoa com Lesão Medular. 2ª ed. Brasília: Ministério da Saúde; 2015. (Biblioteca Virtual em Saúde)
- Rouanet C, Reges D, Rocha E, et al. Traumatic spinal cord injury: current concepts and treatment update. Arq Neuropsiquiatr. 2017. (SciELO)
- Kirshblum S, et al. Characterizing Natural Recovery after Traumatic Spinal Cord Injury. J Neurotrauma. 2021. (PMC)
- Stokum JA, et al. Mechanisms of Traumatic Spinal Cord Injury AIS Grade Conversion (review/analysis). 2025. (Liebert Publishing)
- Ottobock. E-MAG Active (órtese com controle da articulação do joelho). (Ottobock)
- Cyberdyne. HAL (Hybrid Assistive Limb) – descrição do sistema. (cyberdyne.jp)
- Cyberdyne Europe. HAL em reabilitação (SCI). (Cyberdyne Care Robotics GmbH)
- Ekso Bionics. EksoNR (exoesqueleto para reabilitação; inclui SCI). (eksobionics.com)
- FDA / ReWalk. Documentos/clearing para exoesqueleto ReWalk (exemplo de exoesqueleto pessoal com indicação regulatória específica). (FDA Access Data)
- Angelin LG, Carreño MNP, Otoch JP, et al. Regeneration and Plasticity Induced by Epidural Stimulation in a Rodent Model of Spinal Cord Injury. Int J Mol Sci. 2024;25(16):9043. (PubMed)
- Porceban MM, Angelin LG, Gabana E, et al. Time Course of Motor Improvement by Epidural Stimulation After Spinal Cord Injury: An Interim Analysis of a Phase II Trial. J Cent Nerv Syst Dis. 2025. PMCID: PMC12454953. (PubMed)
- Angeli CA, Rejc E, Ugiliweneza B, et al. Activity-based recovery training with spinal cord epidural stimulation improves standing performance in cervical spinal cord injury. J Neuroeng Rehabil. 2025;22(1):101. (PubMed)
- Rowald A, Komi S, Demesmaeker R, et al. Activity-dependent spinal cord neuromodulation rapidly restores trunk and leg motor functions after complete paralysis. Nat Med. 2022;28(2):260-271. (PubMed)
- Lepski G, Milanezi R, Arévalo A. What Determines Success with Robot-Assisted Upper Limb Rehabilitation Following Stroke? A Systematic Review and Meta-Analysis. SSRN. 2023. (SSRN)
- Silva RC, et al. Biomimetic Design of a Tendon-Driven Myoelectric Soft Hand Exoskeleton. Biomimetics. 2023;8(3):317. (MDPI)
- Li J, Lepski G. Cell transplantation for spinal cord injury: a systematic review. Biomed Res Int. 2013;2013:786475. (PubMed)
- Mariano ED, Batista CM, Barbosa BJ, et al. Current perspectives in stem cell therapy for spinal cord repair in humans: a review of work from the past 10 years. Arq Neuropsiquiatr. 2014;72(6):451-456. (PubMed)
- Lepski G. Transplantation of GABAergic precursors into the spinal cord to alleviate neuropathic pain. Ann Palliat Med. 2020. (PubMed)